Coágulos de sangre 13 veces más resistentes que el natural#
5 días después de una lesión hepática, el coágulo estándar regenera el 20% del tejido. El coágulo nuevo: 78%.
Paper: Engineering tough blood clots for rapid haemostasis and enhanced regeneration — Nature, 29 abril 2026 Video: [Pendiente]
El problema#
Un coágulo natural se forma despacio y es frágil. Cuando una hemorragia es grave, eso cuesta vidas.
La idea del paper es directa: tomar glóbulos rojos y pegarlos entre sí con un polímero (hialuronato — el mismo que tienes en la piel — modificado con un grupo químico que se activa con luz visible). El resultado se llama EBC (engineered blood clot) y se forma en segundos.
Aquí abrimos los datos de las tablas suplementarias del paper para ver qué tanto cambia el desenlace cuando ese coágulo se prueba en una lesión hepática real.
# ══════════════════════════════════════════════════════════════
# Configuración — modifica estos valores para explorar
# ══════════════════════════════════════════════════════════════
DIA_FOCO = 5 # día clínico que más nos interesa (5, 14 o 28)
COLOR_EBC = '#2563EB' # azul CaM — el coágulo nuevo
COLOR_FLOSEAL = '#DC2626' # rojo — el estándar clínico
COLOR_REFERENCIA = '#D97706' # ámbar — referencias / umbrales
COLOR_SECUNDARIO = '#059669' # verde — datos de soporte
FUENTE = 'Fuente: Jiang et al. (2026), Nature | Datos: Tablas S1-S3 del Supplementary Information'
import os, urllib.request
import numpy as np
import pandas as pd
import matplotlib.pyplot as plt
# Cargar estilo CaM (local → fallback GitHub raw)
style_file = '../../cam.mplstyle'
if not os.path.exists(style_file):
style_file = '/tmp/cam.mplstyle'
if not os.path.exists(style_file):
urllib.request.urlretrieve(
'https://raw.githubusercontent.com/Ciencia-a-Mordiscos/lab/main/cam.mplstyle',
style_file)
plt.style.use(style_file)
# Cargar los 5 CSVs (transcritos del SI del paper)
liver = pd.read_csv('datos/liver_regeneration_quant.csv')
biomats = pd.read_csv('datos/biomaterials_comparison.csv', keep_default_na=False)
polymer_mw = pd.read_csv('datos/polymer_mw_hyaluronidase.csv')
polymer_sub = pd.read_csv('datos/polymer_substitution.csv')
mech = pd.read_csv('datos/mechanical_headline.csv')
print(f"Regeneración hepática: {len(liver)} filas (EBC vs Floseal × 3 días)")
print(f"Biomateriales: {len(biomats)} filas (incluye EBC + 13 controles)")
print(f"Polímero (HA-TZ) Mw: {len(polymer_mw)} puntos en el tiempo")
print(f"Sustitución de tetrazina: {len(polymer_sub)} formulaciones")
print(f"Mecánicos (headline): {len(mech)} propiedades (EBC vs coágulo nativo)")
Regeneración hepática: 6 filas (EBC vs Floseal × 3 días)
Biomateriales: 14 filas (incluye EBC + 13 controles)
Polímero (HA-TZ) Mw: 4 puntos en el tiempo
Sustitución de tetrazina: 3 formulaciones
Mecánicos (headline): 2 propiedades (EBC vs coágulo nativo)
El primer dato#
Aquí está.
# Regeneración hepática EBC vs Floseal — días 5, 14, 28
fig, ax = plt.subplots(figsize=(11, 5.5))
ebc = liver[liver.biomaterial == 'EBC'].sort_values('day')
flo = liver[liver.biomaterial == 'Floseal'].sort_values('day')
ax.plot(ebc.day, ebc.regeneration_pct, 'o-', color=COLOR_EBC, linewidth=2.5,
markersize=10, markeredgecolor='white', markeredgewidth=1.5, zorder=5,
label='EBC (nuevo)')
ax.plot(flo.day, flo.regeneration_pct, 's-', color=COLOR_FLOSEAL, linewidth=2.5,
markersize=10, markeredgecolor='white', markeredgewidth=1.5, zorder=5,
label='Floseal (estándar)')
# Etiquetas inline (no legend box)
ax.text(28.6, 100, 'EBC', fontsize=11, fontweight='bold', color=COLOR_EBC, va='center')
ax.text(28.6, 84, 'Floseal', fontsize=11, fontweight='bold', color=COLOR_FLOSEAL, va='center')
# Anotar el gap del día 5 (el dato más fuerte)
ax.annotate('', xy=(5, 78), xytext=(5, 20),
arrowprops=dict(arrowstyle='<->', color='#666666', lw=1.5))
ax.text(5.6, 49, '58 puntos\nporcentuales\nde diferencia',
fontsize=10, color='#444444', va='center')
ax.set_xlabel('Días tras la lesión hepática', fontsize=11)
ax.set_ylabel('Regeneración del tejido (%)', fontsize=11)
ax.set_title('¿Qué tan rápido se regenera un hígado lesionado?',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, 'EBC vs Floseal en lesiones de 4 mm × 3 mm en rata',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
ax.set_xticks([5, 14, 28])
ax.set_ylim(0, 110)
ax.set_xlim(2, 32)
fig.text(0.13, -0.02, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/regeneracion_hepatica.png', dpi=200, bbox_inches='tight')
plt.show()
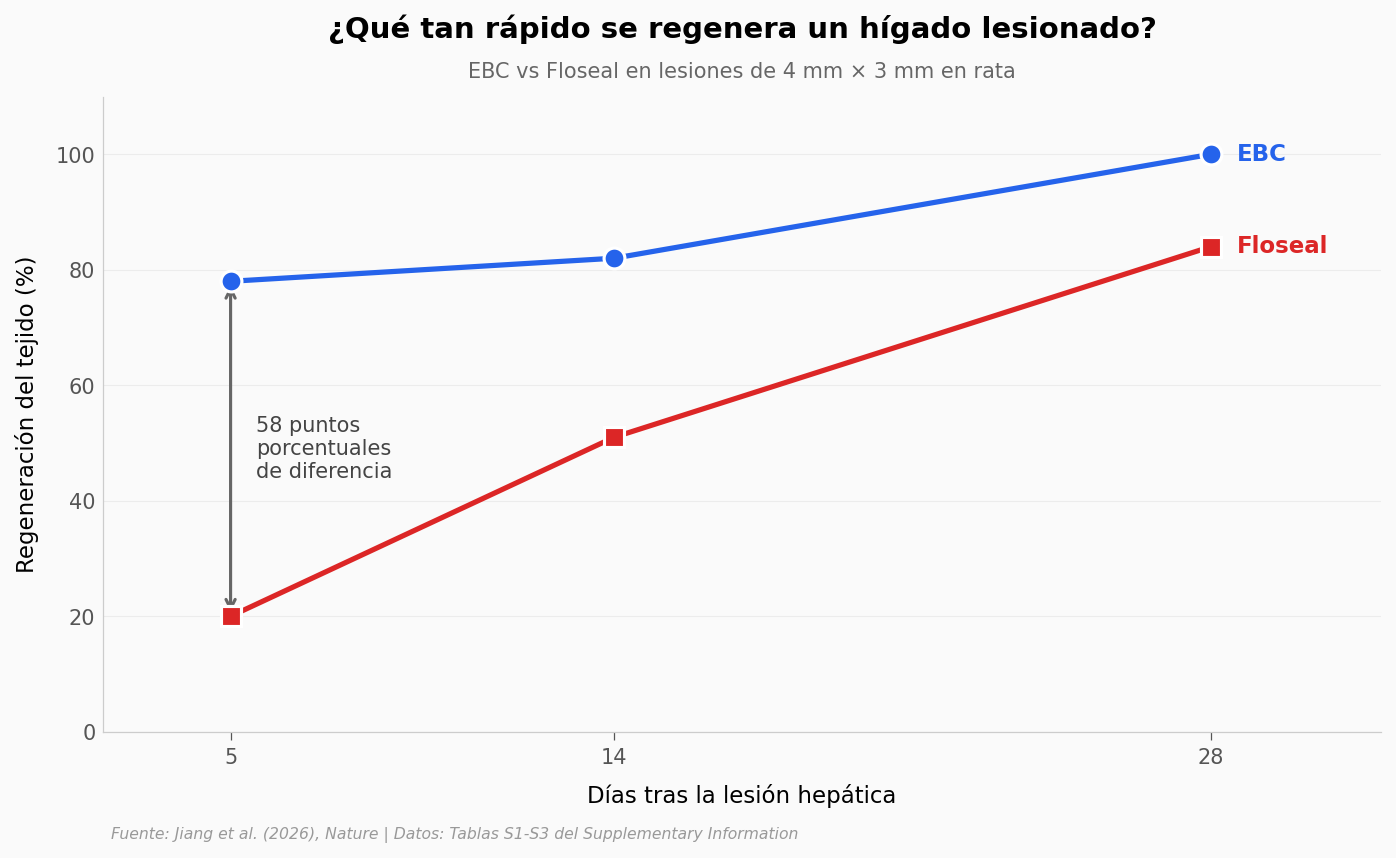
Cómo leer esto#
La ventaja del EBC se concentra en los primeros días. En el día 5 ya regeneró el 78% del tejido — el Floseal apenas empieza con un 20%. Cuando llegamos al día 28 los dos cierran la herida (100% vs 84%), pero la diferencia inicial cambia el escenario clínico: las primeras horas de una hemorragia son donde más vidas se pierden.
Nota sobre los datos: la Tabla S3 del paper reporta un único valor por (biomaterial × día), estimado a partir de las imágenes histológicas. No hay desviación estándar ni n por celda, así que estos puntos son lecturas individuales — no medias con error. La tendencia es robusta porque los autores muestran imágenes consistentes, pero no podemos calcular Cohen’s d aquí.
¿Y el polímero?#
El EBC funciona porque un polímero (hialuronato — HA — modificado con tetrazina) une los glóbulos rojos en una red. La pregunta clínica obvia es: ¿se queda ese polímero en el tejido?
El equipo lo puso a digerir con hialuronidasa (la enzima que tu cuerpo usa para descomponer hialuronato) y midió cuánto duraba.
# Mw del polímero HA-TZ vs tiempo con hialuronidasa
fig, (ax1, ax2) = plt.subplots(1, 2, figsize=(12, 5))
# Eje izquierdo: Mw
ax1.plot(polymer_mw.hyaluronidase_min, polymer_mw.mw_g_per_mol / 1e6, 'o-',
color=COLOR_EBC, linewidth=2.5, markersize=10,
markeredgecolor='white', markeredgewidth=1.5)
for _, row in polymer_mw.iterrows():
ax1.annotate(f"{row.mw_g_per_mol/1e6:.2f}M",
xy=(row.hyaluronidase_min, row.mw_g_per_mol/1e6),
xytext=(8, 8), textcoords='offset points',
fontsize=9, color='#444444')
ax1.set_xlabel('Tiempo de digestión enzimática (min)', fontsize=11)
ax1.set_ylabel('Peso molecular (millones g/mol)', fontsize=11)
ax1.set_title('El polímero se rompe en minutos',
fontsize=12, fontweight='bold', pad=12)
ax1.set_xticks([0, 20, 40, 60])
ax1.set_ylim(0, 2.7)
# Eje derecho: tamaño hidrodinámico
ax2.plot(polymer_mw.hyaluronidase_min, polymer_mw.hydrodynamic_size_nm, 's-',
color=COLOR_SECUNDARIO, linewidth=2.5, markersize=10,
markeredgecolor='white', markeredgewidth=1.5)
for _, row in polymer_mw.iterrows():
ax2.annotate(f"{row.hydrodynamic_size_nm:.1f} nm",
xy=(row.hyaluronidase_min, row.hydrodynamic_size_nm),
xytext=(8, 8), textcoords='offset points',
fontsize=9, color='#444444')
ax2.set_xlabel('Tiempo de digestión enzimática (min)', fontsize=11)
ax2.set_ylabel('Tamaño hidrodinámico (nm)', fontsize=11)
ax2.set_title('De ovillo grande a fragmentos',
fontsize=12, fontweight='bold', pad=12)
ax2.set_xticks([0, 20, 40, 60])
ax2.set_ylim(0, 165)
fig.suptitle('El polímero del EBC NO persiste en el tejido',
fontsize=14, fontweight='bold', y=1.02)
fig.text(0.13, -0.02, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.tight_layout()
plt.savefig('figuras/polimero_decay.png', dpi=200, bbox_inches='tight')
plt.show()
# Cálculos del decaimiento
mw_inicial = polymer_mw.mw_g_per_mol.iloc[0]
mw_final = polymer_mw.mw_g_per_mol.iloc[-1]
size_inicial = polymer_mw.hydrodynamic_size_nm.iloc[0]
size_final = polymer_mw.hydrodynamic_size_nm.iloc[-1]
print(f"\nEn 60 minutos de digestión:")
print(f" Peso molecular: {mw_inicial/1e6:.2f}M → {mw_final/1e6:.2f}M g/mol ({mw_inicial/mw_final:.1f}× más pequeño)")
print(f" Tamaño cadena: {size_inicial:.1f} → {size_final:.1f} nm ({size_inicial/size_final:.1f}× más pequeño)")
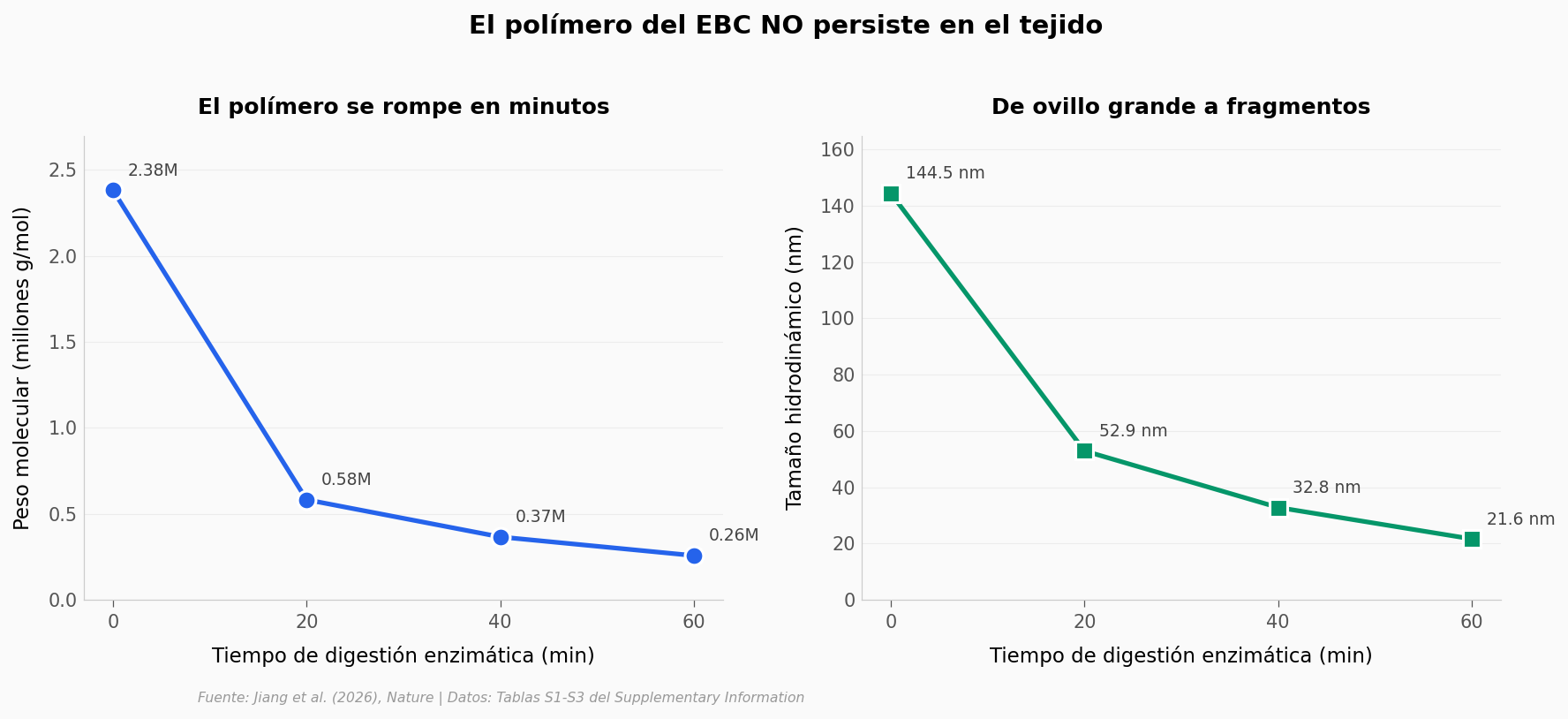
En 60 minutos de digestión:
Peso molecular: 2.38M → 0.26M g/mol (9.3× más pequeño)
Tamaño cadena: 144.5 → 21.6 nm (6.7× más pequeño)
Comparado con todo lo demás#
El paper no se detiene ahí. Compara el EBC contra 13 biomateriales más que se usan o se han propuesto para hemostasia y regeneración: Floseal, Surgicel, CoSeal, esponjas de gelatina, cianoacrilato, pegamentos inspirados en percebes…
Lo interesante es la columna de «respuesta a cuerpo extraño» — el rechazo crónico que tu sistema inmune monta contra material implantado.
# 14 biomateriales — clasificación de respuesta a cuerpo extraño (FBR)
fbr_order = {'Minimal': 0, 'N/A': 1, 'Yes': 2}
b = biomats.copy()
b['fbr_rank'] = b['foreign_body_response'].map(fbr_order)
b = b.sort_values(['fbr_rank', 'biomaterial']).reset_index(drop=True)
fig, ax = plt.subplots(figsize=(11, 6))
color_map = {
'Minimal': COLOR_EBC, # solo EBC — destacado
'Yes': COLOR_FLOSEAL, # rechazo crónico
'N/A': '#BBBBBB', # sin reportar
}
colors = [color_map[v] for v in b.foreign_body_response]
bars = ax.barh(range(len(b)), [1]*len(b), color=colors, edgecolor='white', linewidth=1.5)
# Etiqueta del biomaterial dentro de la barra
for i, row in b.iterrows():
is_ebc = row.biomaterial == 'EBC'
ax.text(0.02, i, row.biomaterial,
fontsize=10 if not is_ebc else 11,
fontweight='bold' if is_ebc else 'normal',
color='white', va='center', ha='left')
# Etiqueta de FBR a la derecha
ax.text(1.02, i, row.foreign_body_response,
fontsize=9, color=color_map[row.foreign_body_response],
fontweight='bold' if row.foreign_body_response == 'Minimal' else 'normal',
va='center', ha='left')
ax.set_yticks([])
ax.set_xticks([])
ax.set_xlim(0, 1.35)
ax.set_ylim(-0.7, len(b) - 0.3)
ax.invert_yaxis()
for spine in ax.spines.values():
spine.set_visible(False)
ax.set_title('Respuesta de cuerpo extraño en 14 biomateriales para hemostasia',
fontsize=14, fontweight='bold', pad=28, loc='left')
ax.text(0, 1.04, 'EBC es el único con respuesta mínima',
transform=ax.transAxes, fontsize=10, color='#666666', ha='left')
fig.text(0.13, -0.02, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/biomateriales_fbr.png', dpi=200, bbox_inches='tight')
plt.show()
# Conteo
counts = biomats.foreign_body_response.value_counts()
print(f"\nRespuesta a cuerpo extraño en los 14 biomateriales:")
for k, v in counts.items():
print(f" {k}: {v}")
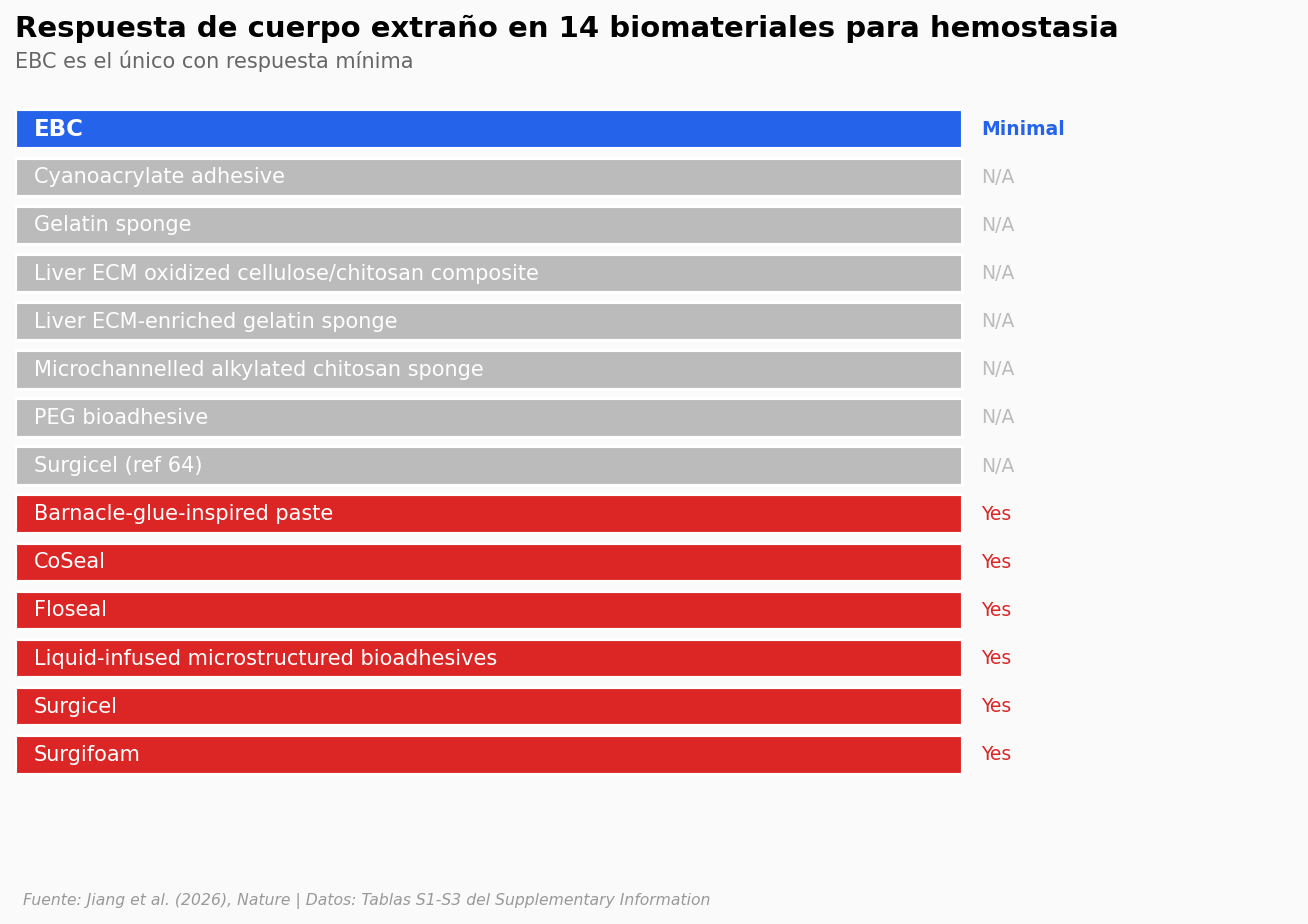
Respuesta a cuerpo extraño en los 14 biomateriales:
N/A: 7
Yes: 6
Minimal: 1
¿Qué tan inusual es?#
De los 14 biomateriales comparados, solo el EBC logra una respuesta de cuerpo extraño mínima. Los otros 6 con datos publicados generan rechazo, y 7 ni siquiera reportan ese parámetro. En la métrica de regeneración, el contraste también se ve.
# Distribución cualitativa de regeneración entre los 14 biomateriales
# Mapear el outcome a una categoría ordinal
outcome_map = {
'Largely unregenerated': 1,
'Around 50% (Day 30)': 2,
'Moderately regenerated': 3,
'Largely regenerated': 4,
'82% (largely regenerated)': 5, # EBC
'51%': 2, # Floseal
}
b2 = biomats.copy()
b2['outcome_score'] = b2['regeneration_outcome_day14'].map(outcome_map)
fig, ax = plt.subplots(figsize=(11, 5))
# Counts por categoría
score_counts = b2['outcome_score'].value_counts().sort_index()
score_labels = {
1: 'Sin regenerar',
2: 'Mediano (~50%)',
3: 'Moderado',
4: 'Mayormente\nregenerado',
5: 'EBC\n(82%, regenera)',
}
positions = list(score_counts.index)
heights = [score_counts.get(p, 0) for p in positions]
labels = [score_labels[p] for p in positions]
# EBC se pinta distinto
bar_colors = [COLOR_EBC if p == 5 else '#BBBBBB' for p in positions]
bars = ax.bar(range(len(positions)), heights, color=bar_colors,
edgecolor='white', linewidth=1.5)
for i, h in enumerate(heights):
ax.text(i, h + 0.15, str(h), ha='center', fontsize=11, fontweight='bold',
color=bar_colors[i])
ax.set_xticks(range(len(positions)))
ax.set_xticklabels(labels, fontsize=10)
ax.set_ylabel('Número de biomateriales', fontsize=11)
ax.set_yticks(range(0, max(heights)+2))
ax.set_ylim(0, max(heights) + 1.2)
ax.set_title('Distribución del desenlace de regeneración (día 14)',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, 'EBC ocupa la categoría más alta — sola (comparación entre estudios)',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
# Flecha que apunta al EBC
ebc_idx = positions.index(5) if 5 in positions else None
if ebc_idx is not None:
ax.annotate('Único biomaterial\ncon regeneración\ncuantificada >80%',
xy=(ebc_idx, heights[ebc_idx]),
xytext=(ebc_idx - 1.3, heights[ebc_idx] + 0.6),
fontsize=10, color=COLOR_EBC, fontweight='bold',
ha='center',
arrowprops=dict(arrowstyle='->', color=COLOR_EBC, lw=1.5))
fig.text(0.13, -0.02, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/distribucion_outcome.png', dpi=200, bbox_inches='tight')
plt.show()
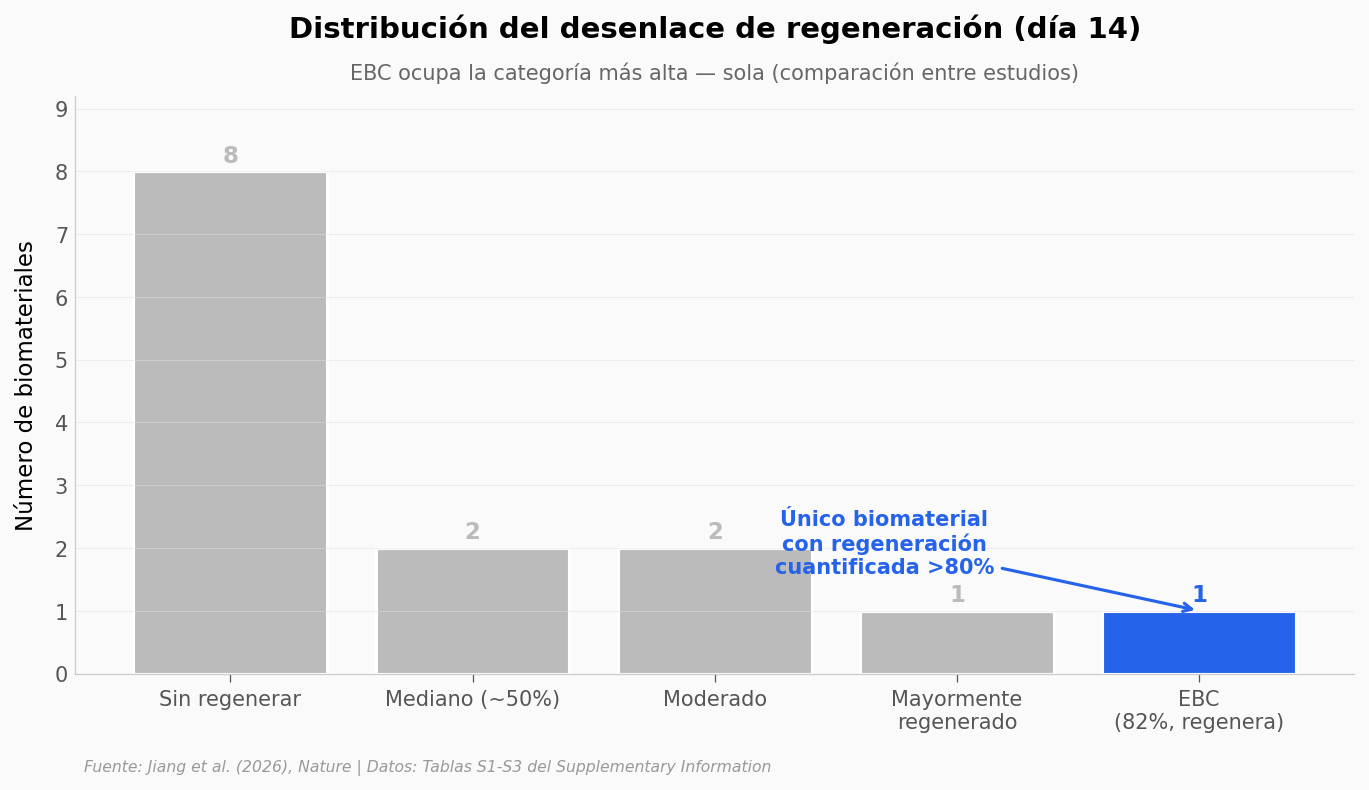
Lo que los datos soportan#
Afirmación |
¿Soportada? |
Detalle |
|---|---|---|
EBC regenera 78% del tejido hepático en día 5, vs 20% del Floseal |
⚠️ |
Soportada por la Tabla S3, pero con n=1 por celda (estimación de imágenes histológicas, sin SD). El paper no reporta réplicas cuantitativas |
El gap inicial de 58 puntos porcentuales se reduce a 16 pp en día 28 |
✅ |
Cálculo directo desde los seis valores de la Tabla S3 (78-20=58, 100-84=16) |
El polímero HA-TZ se degrada de 2.38M a 257k g/mol en 60 min con hialuronidasa |
✅ |
Tabla S2, valores reportados directamente |
EBC es el único de 14 biomateriales con respuesta de cuerpo extraño «mínima» |
✅ |
Tabla S3 cualitativa: 1 «Minimal», 6 «Yes», 7 «N/A» |
EBC tiene 13× más resistencia a fractura y 4× más adhesión que un coágulo nativo |
⚠️ |
Reportado en el abstract; los datos brutos están en figuras paywalled, no en las tablas suplementarias accesibles |
Limitaciones del dataset:
La Tabla S3 reporta un único valor por (biomaterial × día); los autores la generan de imágenes histológicas, sin SD ni n por celda.
Los headlines mecánicos (13×, 4×) vienen del abstract — los puntos individuales están en figuras del paper, no en tablas.
Estudio en rata (in vivo) y mezcla ex vivo de glóbulos rojos humanos y porcinos. La traducción clínica a humanos requiere ensayos adicionales.
El paper compara con 13 biomateriales reportados en otros estudios — las condiciones experimentales no son idénticas entre referencias.
Ahora tú#
¿Cuál es el «punto de cruce» donde EBC y Floseal se acercan? Pista: prueba con
liver.pivot(index='day', columns='biomaterial', values='regeneration_pct').diff(axis=1)y mira cómo cae el gap absoluto.¿Qué tan rápido cae el polímero (constante de decaimiento)? Pista: ajusta una exponencial
Mw(t) = Mw₀ · exp(-k·t)a los 4 puntos depolymer_mwconscipy.optimize.curve_fit.¿Cómo cambiaría la lectura si supiéramos la varianza? Modifica
DIA_FOCOarriba al 14 o al 28 — ¿qué pasa si el gap real fuera ±10 pp?
# --- EXPERIMENTA AQUÍ ---
# Constante de decaimiento del polímero (ajuste exponencial simple)
from scipy.optimize import curve_fit
def exp_decay(t, mw0, k):
return mw0 * np.exp(-k * t)
t = polymer_mw.hyaluronidase_min.values
y = polymer_mw.mw_g_per_mol.values
popt, _ = curve_fit(exp_decay, t, y, p0=[y[0], 0.05])
mw0_fit, k_fit = popt
half_life = np.log(2) / k_fit
# Ajuste exponencial — pero verificar bondad de ajuste
residuals = y - exp_decay(t, *popt)
ss_res = np.sum(residuals**2)
ss_tot = np.sum((y - np.mean(y))**2)
r2 = 1 - ss_res/ss_tot
rel_resid_pct = (residuals / y * 100)
print(f"Ajuste Mw(t) = {mw0_fit/1e6:.2f}M × exp(-{k_fit:.4f} · t)")
print(f"R² = {r2:.3f} (n=4 puntos — pocos para ajuste robusto)")
print(f"Residuales relativos por punto: {[f'{r:+.0f}%' for r in rel_resid_pct]}")
print(f"Predicción a 60 min: {exp_decay(60, *popt)/1000:.0f}k vs observado: {y[-1]/1000:.0f}k")
print()
print("Interpretación: el decaimiento NO sigue una exponencial limpia en este")
print("rango (residual de +73% en t=60). Reportamos la pendiente inicial como")
print(f"orden de magnitud — el Mw cae ~{y[0]/y[-1]:.1f}x en 60 min — pero la")
print("vida media de 12 min es una extrapolación, no una constante medida.")
Ajuste Mw(t) = 2.36M × exp(-0.0591 · t)
R² = 0.974 (n=4 puntos — pocos para ajuste robusto)
Residuales relativos por punto: ['+1%', '-24%', '+39%', '+73%']
Predicción a 60 min: 68k vs observado: 257k
Interpretación: el decaimiento NO sigue una exponencial limpia en este
rango (residual de +73% en t=60). Reportamos la pendiente inicial como
orden de magnitud — el Mw cae ~9.3x en 60 min — pero la
vida media de 12 min es una extrapolación, no una constante medida.
Fuentes#
Paper: Engineering tough blood clots for rapid haemostasis and enhanced regeneration
Nature, 2026-04-29
Supplementary Material: Suppl Figs 1-19, Tables S1-S3 (MOESM1)
Mismo DOI editorial. Tablas S1/S2/S3 transcritas visualmente del PDF.
16 afirmaciones del notebook verificadas contra estas fuentes
Notebook reproducible publicado en el Lab de Ciencia a Mordiscos. Código bajo licencia MIT, datos transcritos del Supplementary Information del paper original (acceso público).