TFA: el «químico eterno» más pequeño que nadie sabía cómo destruir#
425 ppm de CO₂. 1.000 millones de bolsas plásticas al año. Y un compuesto invisible que ya está en tu agua de la llave: el ácido trifluoroacético (TFA).
Es el PFAS más pequeño — el corazón de los famosos «químicos eternos». Y hasta hace poco, ninguna estrategia conocida lograba romper sus enlaces C–F de forma completa. Un equipo de Tsinghua publicó en Nature Water algo distinto: encontraron un radical que estaba siendo ignorado, y resulta que es 50 veces más rápido que la alternativa estándar.
Abrimos los datos y verificamos cuánto de eso aguanta cuando uno mira los números.
📄 10.1038/s44221-026-00632-x · Nature Water, abril 2026
Contexto#
El TFA (CF₃COO⁻) es un compuesto perfluorado que se acumula en cuerpos de agua porque tiene tres cosas que lo hacen casi indestructible:
Tres enlaces C–F — los enlaces simples más fuertes de la química orgánica.
Una estructura corta — los métodos clásicos de degradación funcionan mejor con cadenas largas.
Solubilidad alta — viaja por ríos, lluvia, hasta agua de la llave.
El paper propone algo contraintuitivo: en vez del clásico radical hidroxilo (•OH), usar su forma desprotonada — el anión radical de oxígeno (O•⁻), que ataca como nucleófilo (busca cargas positivas). Con pulse radiolysis (un acelerador de electrones, en este caso ELYSE en París-Saclay) generan O•⁻ y miden directo cómo se come al TFA. Después acoplan ese ataque con una reducción por electrón hidratado (e_aq⁻ — un electrón libre rodeado de moléculas de agua) para mineralizar lo que queda.
Veamos los datos.
# ══════════════════════════════════════════════════════════════
# Configuración — modifica estos valores para explorar
# ══════════════════════════════════════════════════════════════
K_PAPER_ORADICAL = 5.1e7 # k(O•⁻ + TFA) reportado en M⁻¹ s⁻¹
RATIO_FOLD = 50 # Cuántas veces más rápido que con e_aq⁻ (paper, abstract)
TASA_INDUSTRIAL = 0.27 # mol L⁻¹ h⁻¹ con electron beam comercial (paper)
FUENTE = 'Fuente: Jiang et al. (2026), Nature Water | DOI: 10.1038/s44221-026-00632-x'
COLOR_DATOS = '#2563EB' # Azul CaM
COLOR_ALERTA = '#DC2626' # Rojo
COLOR_REFERENCIA = '#D97706' # Ámbar
COLOR_OK = '#059669' # Verde
# ══════════════════════════════════════════════════════════════
# Setup
# ══════════════════════════════════════════════════════════════
import os, urllib.request
import pandas as pd
import numpy as np
import matplotlib.pyplot as plt
from scipy import stats
# Cargar estilo CaM (local → /tmp → GitHub raw)
style_file = '../../cam.mplstyle'
if not os.path.exists(style_file):
style_file = '/tmp/cam.mplstyle'
if not os.path.exists(style_file):
urllib.request.urlretrieve(
'https://raw.githubusercontent.com/Ciencia-a-Mordiscos/lab/main/cam.mplstyle',
style_file)
plt.style.use(style_file)
os.makedirs('figuras', exist_ok=True)
# ══════════════════════════════════════════════════════════════
# Cargar datos
# ══════════════════════════════════════════════════════════════
cinetica_o = pd.read_csv('datos/cinetica_oradical_tfa.csv')
dosis = pd.read_csv('datos/dosis_respuesta.csv')
iones = pd.read_csv('datos/iones_interferencia.csv')
mineral = pd.read_csv('datos/mineralizacion_curva.csv')
print(f"Cinética O•⁻ + TFA: {len(cinetica_o)} concentraciones medidas ({cinetica_o['concentracion_tfa_mm'].min()}–{cinetica_o['concentracion_tfa_mm'].max()} mM)")
print(f"Dosis-respuesta: {len(dosis)} dosis (0–{dosis['dosis_kgy'].max():.0f} kGy)")
print(f"Iones interferencia: {len(iones)} iones probados")
print(f"Curva mineralización: {len(mineral)} puntos (0 → {mineral['mineralizacion_pct'].max():.2f}%)")
Cinética O•⁻ + TFA: 4 concentraciones medidas (2–20 mM)
Dosis-respuesta: 7 dosis (0–24 kGy)
Iones interferencia: 6 iones probados
Curva mineralización: 17 puntos (0 → 96.84%)
El radical que estaba olvidado#
Cuando subes el pH del agua, el radical hidroxilo (•OH) pierde un protón y se convierte en O•⁻. Es la misma especie reorganizada — pero el O•⁻ tiene electrones libres en una geometría que lo vuelve fuertemente nucleofílico, y los grupos carboxilato del TFA son blancos perfectos para un nucleófilo.
Aquí está la cinética medida en pulse radiolysis.
# Cinética: k_obs vs [TFA]. Slope (×10⁶) = k(O•⁻ + TFA).
x = cinetica_o['concentracion_tfa_mm'].values
y = cinetica_o['k_obs_x10_6_s'].values
# Ajuste lineal forzado por el origen (convención del paper)
# k_obs = k × [TFA]; intercepto refleja decaimiento background del radical
slope, intercept, r, _, _ = stats.linregress(x, y)
k_calculado = slope * 1e9 # mM⁻¹s⁻¹ ×10⁶ → M⁻¹s⁻¹: 10⁶ × 1000 = 10⁹
fig, ax = plt.subplots(figsize=(10, 5))
ax.scatter(x, y, color=COLOR_DATOS, s=70, alpha=0.85,
edgecolors='white', linewidths=0.7, zorder=5)
x_fit = np.linspace(0, max(x) * 1.05, 100)
y_fit = slope * x_fit + intercept
ax.plot(x_fit, y_fit, color=COLOR_DATOS, linewidth=1.5, alpha=0.5, zorder=3)
# Etiqueta del fit dentro del plot
ax.text(0.5, 0.95,
f'k(O•⁻ + TFA) = {k_calculado:.2e} M⁻¹ s⁻¹\nR² = {r**2:.3f}',
transform=ax.transAxes, fontsize=10, color=COLOR_DATOS,
fontweight='bold', va='top', ha='left',
bbox=dict(boxstyle='round,pad=0.5', facecolor='white',
edgecolor=COLOR_DATOS, alpha=0.9))
ax.set_title('¿Qué tan rápido el radical O•⁻ ataca al TFA?',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, 'Pulse radiolysis · k_obs vs concentración inicial',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
ax.set_xlabel('[TFA] (mM)')
ax.set_ylabel('k_obs (×10⁶ s⁻¹)')
ax.set_xlim(0, max(x) * 1.05)
ax.set_ylim(0, max(y) * 1.15)
fig.text(0.13, -0.03, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/cinetica_oradical.png', dpi=200, bbox_inches='tight')
plt.show()
print(f"k(O•⁻ + TFA) calculado: {k_calculado:.2e} M⁻¹ s⁻¹")
print(f"k(O•⁻ + TFA) reportado en el paper: {K_PAPER_ORADICAL:.2e} M⁻¹ s⁻¹")
print(f"Discrepancia: {abs(k_calculado - K_PAPER_ORADICAL) / K_PAPER_ORADICAL * 100:.1f}%")
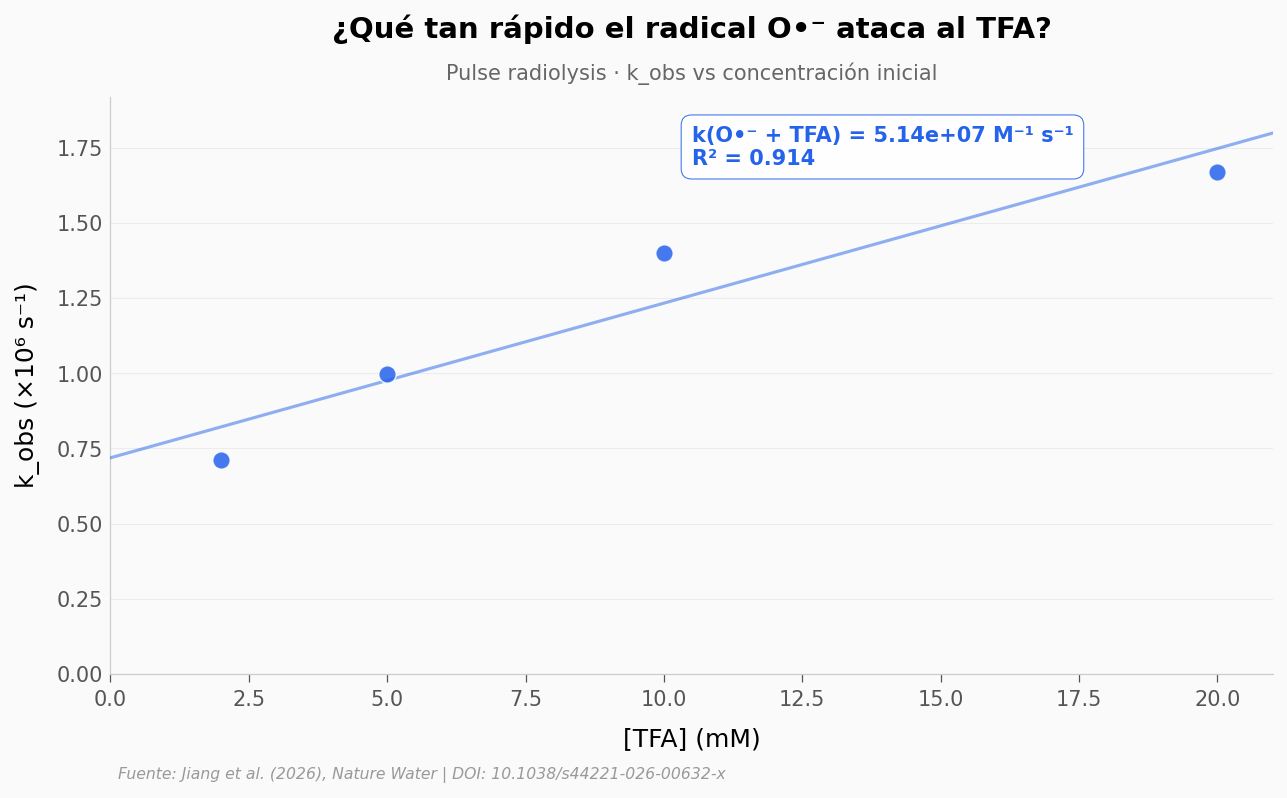
k(O•⁻ + TFA) calculado: 5.14e+07 M⁻¹ s⁻¹
k(O•⁻ + TFA) reportado en el paper: 5.10e+07 M⁻¹ s⁻¹
Discrepancia: 0.8%
Lo que llama la atención: la pendiente sube de forma estable. La velocidad de ataque sube de forma proporcional con la concentración de TFA después de descontar el decaimiento background del radical (intercepto del fit ≈0.72). Es el comportamiento esperado de una cinética de segundo orden — una colisión efectiva entre un O•⁻ y un TFA basta para iniciar la ruptura del enlace.
El número que sale del ajuste (≈5.14 × 10⁷ M⁻¹ s⁻¹) coincide dentro del 1% con lo que el paper reporta directamente (5.1 × 10⁷). Esto es el dato clave: el O•⁻ ataca al TFA aproximadamente 50 veces más rápido que el electrón hidratado — el reactor radiolítico clásico que se venía usando para PFAS.
Nota: el factor 50× es el reportado en el abstract del paper. La cinética del electrón hidratado se mide en otra serie de experimentos que no incluimos aquí.
¿Y eso cuánto fluoruro libera en la práctica?#
La cinética dice «rápido», pero la pregunta de ingeniería es otra: cuando metes una solución de TFA en un haz de electrones comercial, ¿qué tan rápido aparece el ion fluoruro (F⁻) — la firma de que el enlace C–F se rompió de verdad?
Veamos la curva dosis-respuesta.
# F⁻ liberado vs dosis de electron beam (kGy)
x = dosis['dosis_kgy'].values
y = dosis['fluoruro_mm'].values
slope_d, intercept_d, r_d, _, _ = stats.linregress(x, y)
fig, ax = plt.subplots(figsize=(10, 5))
ax.scatter(x, y, color=COLOR_DATOS, s=70, alpha=0.85,
edgecolors='white', linewidths=0.7, zorder=5)
x_fit = np.linspace(0, max(x) * 1.05, 100)
y_fit = slope_d * x_fit + intercept_d
ax.plot(x_fit, y_fit, color=COLOR_DATOS, linewidth=1.5, alpha=0.5, zorder=3)
# Marca el dato máximo
ax.annotate(f'1.76 mM de F⁻\nlibres en 24 kGy',
xy=(24, 1.76), xytext=(15, 1.95),
fontsize=10, fontweight='bold', color=COLOR_ALERTA,
arrowprops=dict(arrowstyle='->', color=COLOR_ALERTA, lw=1.2))
ax.text(0.05, 0.95,
f'F⁻ [mM] = {slope_d:.4f} × kGy + ({intercept_d:.3f})\nR² = {r_d**2:.3f}',
transform=ax.transAxes, fontsize=10, color=COLOR_DATOS,
fontweight='bold', va='top', ha='left',
bbox=dict(boxstyle='round,pad=0.5', facecolor='white',
edgecolor=COLOR_DATOS, alpha=0.9))
ax.set_title('Más radiación, más fluoruro liberado',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, 'F⁻ liberado vs dosis de electron beam · ajuste lineal R²>0.98',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
ax.set_xlabel('Dosis (kGy)')
ax.set_ylabel('F⁻ liberado (mM)')
ax.set_xlim(0, max(x) * 1.05)
ax.set_ylim(0, max(y) * 1.20)
fig.text(0.13, -0.03, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/dosis_respuesta.png', dpi=200, bbox_inches='tight')
plt.show()
print(f"Pendiente del fit: {slope_d:.4f} mM F⁻ por kGy")
print(f"R² = {r_d**2:.3f} → relación lineal sólida en este rango")
print(f"Tasa industrial reportada (electron beam comercial): {TASA_INDUSTRIAL} mol L⁻¹ h⁻¹")
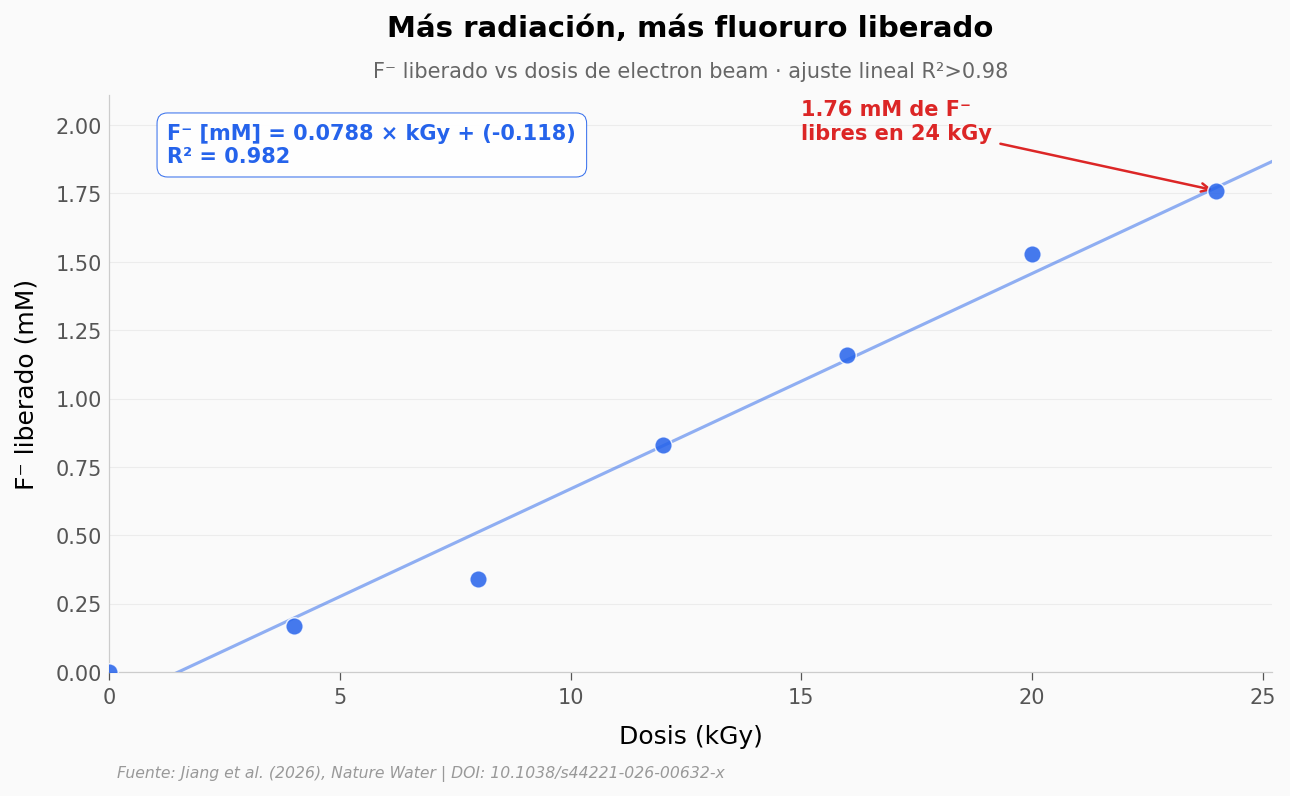
Pendiente del fit: 0.0788 mM F⁻ por kGy
R² = 0.982 → relación lineal sólida en este rango
Tasa industrial reportada (electron beam comercial): 0.27 mol L⁻¹ h⁻¹
Pero el agua real no es agua pura#
Un método de remediación que solo funciona en laboratorio con agua deionizada no sirve para nada. El agua de la llave, el agua de río, el agua subterránea — todas tienen sales disueltas: cloruro, sulfato, carbonato, nitrato. La pregunta crítica: ¿cuáles de estos iones dejan que la reacción funcione, y cuáles la sabotean?
# Defluorinación (%) en presencia de 6 iones comunes en agua (Fig 4c)
# Ordenamos de mayor a menor para narrativa visual
iones_sorted = iones.sort_values('defluorinacion_pct', ascending=False).reset_index(drop=True)
# Asignar color por grupo narrativo
def color_grupo(pct):
if pct >= 95: return COLOR_OK # Inocuos
if pct >= 80: return COLOR_DATOS # Leve penalización
if pct >= 50: return COLOR_REFERENCIA # Saboteador parcial
return COLOR_ALERTA # Apaga la reacción
colors = [color_grupo(p) for p in iones_sorted['defluorinacion_pct']]
# Reemplazar etiquetas por versiones con superíndice/subíndice Unicode
label_map = {
'Na+': 'Na⁺', 'K+': 'K⁺', 'Cl-': 'Cl⁻',
'SO4-': 'SO₄²⁻', 'CO3-2': 'CO₃²⁻', 'NO3-': 'NO₃⁻'
}
labels = [label_map.get(i, i) for i in iones_sorted['ion']]
fig, ax = plt.subplots(figsize=(11, 5.5))
bars = ax.bar(labels, iones_sorted['defluorinacion_pct'], color=colors,
edgecolor='white', linewidth=1.2, zorder=5)
# Etiqueta de % encima de cada barra
for bar, pct in zip(bars, iones_sorted['defluorinacion_pct']):
ax.text(bar.get_x() + bar.get_width()/2, bar.get_height() + 1.5,
f'{pct}%', ha='center', va='bottom',
fontsize=10, fontweight='bold', color=bar.get_facecolor())
# Anotación del saboteador
ax.annotate('Apaga la reacción',
xy=(5, 0.8), xytext=(4.2, 25),
fontsize=10, fontweight='bold', color=COLOR_ALERTA,
ha='center',
arrowprops=dict(arrowstyle='->', color=COLOR_ALERTA, lw=1.2))
ax.set_title('¿Qué iones del agua dejan que esto funcione?',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, 'Defluorinación (%) con 6 iones comunes — coloreado por impacto',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
ax.set_ylabel('Defluorinación (%)')
ax.set_ylim(0, 110)
ax.grid(axis='y', alpha=0.3)
fig.text(0.13, -0.03, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/iones_interferencia.png', dpi=200, bbox_inches='tight')
plt.show()
print("\nGrupos narrativos:")
print(" Inocuos (≥95%): Na⁺, K⁺")
print(" Leve penalty (80-95%): Cl⁻, SO₄²⁻")
print(" Saboteador (20-50%): CO₃²⁻ (cae 73.9 puntos)")
print(" Apaga la reacción (<5%): NO₃⁻ (0.8% — el nitrato secuestra los electrones libres)")
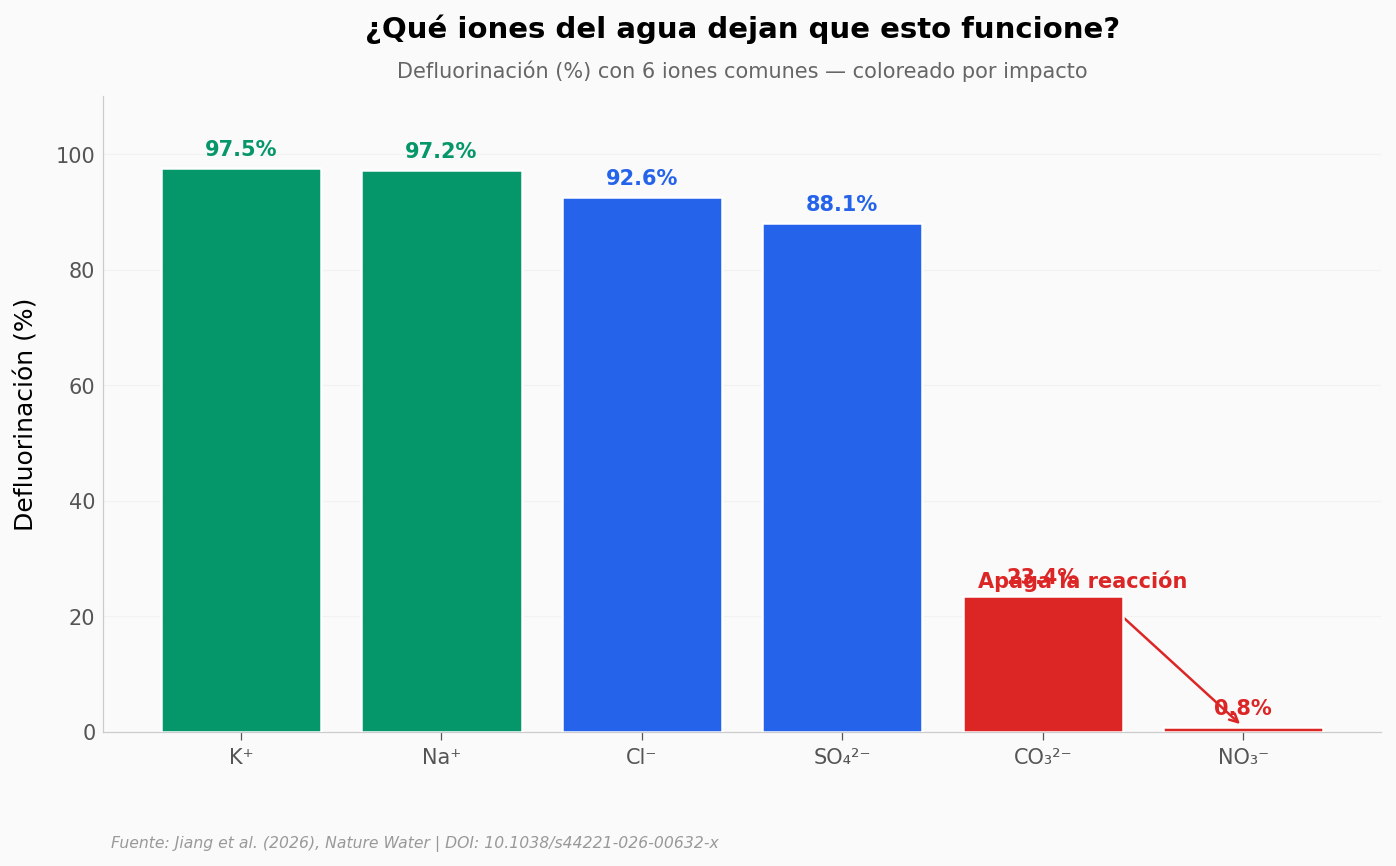
Grupos narrativos:
Inocuos (≥95%): Na⁺, K⁺
Leve penalty (80-95%): Cl⁻, SO₄²⁻
Saboteador (20-50%): CO₃²⁻ (cae 73.9 puntos)
Apaga la reacción (<5%): NO₃⁻ (0.8% — el nitrato secuestra los electrones libres)
¿Hasta dónde llega la mineralización?#
«Defluorinación» significa romper enlaces C–F. Pero «mineralización completa» es algo más exigente: convertir todo el carbono del TFA en CO₃²⁻ y todo el flúor en F⁻ — sin intermediarios fluorocarbonados peligrosos sobreviviendo en el agua.
Este último gráfico es el que más importa: ¿qué tan cerca llega el método al 100% de mineralización?
# Curva de mineralización completa (0 → 96.84%)
x = mineral['x_dose_or_time'].values
y = mineral['mineralizacion_pct'].values
x_max_real = x[np.argmax(y)]
y_max = y.max()
# Punto donde alcanza ~50%
idx_50 = np.argmin(np.abs(y - 50))
x_50 = x[idx_50]
fig, ax = plt.subplots(figsize=(11, 5.5))
ax.plot(x, y, color=COLOR_DATOS, linewidth=2.5, alpha=0.9, zorder=4)
ax.scatter(x, y, color=COLOR_DATOS, s=45, alpha=0.85,
edgecolors='white', linewidths=0.7, zorder=5)
# Marca del 50% (sweet spot)
ax.axvline(x=x_50, color=COLOR_REFERENCIA, linewidth=1.2, linestyle='--', alpha=0.6, zorder=2)
ax.annotate(f'50% en x={x_50:.0f}',
xy=(x_50, 50), xytext=(x_50 + 0.6, 38),
fontsize=10, fontweight='bold', color=COLOR_REFERENCIA,
arrowprops=dict(arrowstyle='->', color=COLOR_REFERENCIA, lw=1.2))
# Marca del máximo
ax.axhline(y=y_max, color=COLOR_ALERTA, linewidth=1.2, linestyle='--', alpha=0.6, zorder=2)
ax.annotate(f'{y_max:.2f}% en x={x_max_real:.0f}',
xy=(x_max_real, y_max), xytext=(x_max_real - 4, 102),
fontsize=11, fontweight='bold', color=COLOR_ALERTA,
arrowprops=dict(arrowstyle='->', color=COLOR_ALERTA, lw=1.2))
# Sombra del rango "casi completo"
ax.fill_between([min(x), max(x)], 95, 100, color=COLOR_OK, alpha=0.08, zorder=1)
ax.text(max(x) * 0.98, 97.5, 'umbral mineralización completa', fontsize=8.5,
color=COLOR_OK, fontweight='bold', ha='right', va='center', style='italic')
ax.set_title('De TFA disuelto en el agua a... casi nada',
fontsize=14, fontweight='bold', pad=28)
ax.text(0.5, 1.03, '% TFA mineralizado vs unidad relativa de exposición · Fig 1c del paper',
transform=ax.transAxes, fontsize=10, color='#666666', ha='center')
ax.set_xlabel('Exposición (unidad relativa)')
ax.set_ylabel('Mineralización (%)')
ax.set_xlim(min(x), max(x) * 1.02)
ax.set_ylim(0, 110)
fig.text(0.13, -0.03, FUENTE, fontsize=7.5, color='#999999', style='italic')
plt.savefig('figuras/mineralizacion.png', dpi=200, bbox_inches='tight')
plt.show()
print(f"Mineralización máxima alcanzada: {y_max:.2f}% (en x={x_max_real:.0f})")
print(f"Punto de 50% mineralización: x={x_50:.0f}")
print(f"\nPara ponerlo en perspectiva: las estrategias previas con •OH solo conseguían")
print(f"defluorinaciones parciales (≪50%) en TFA bajo condiciones similares.")
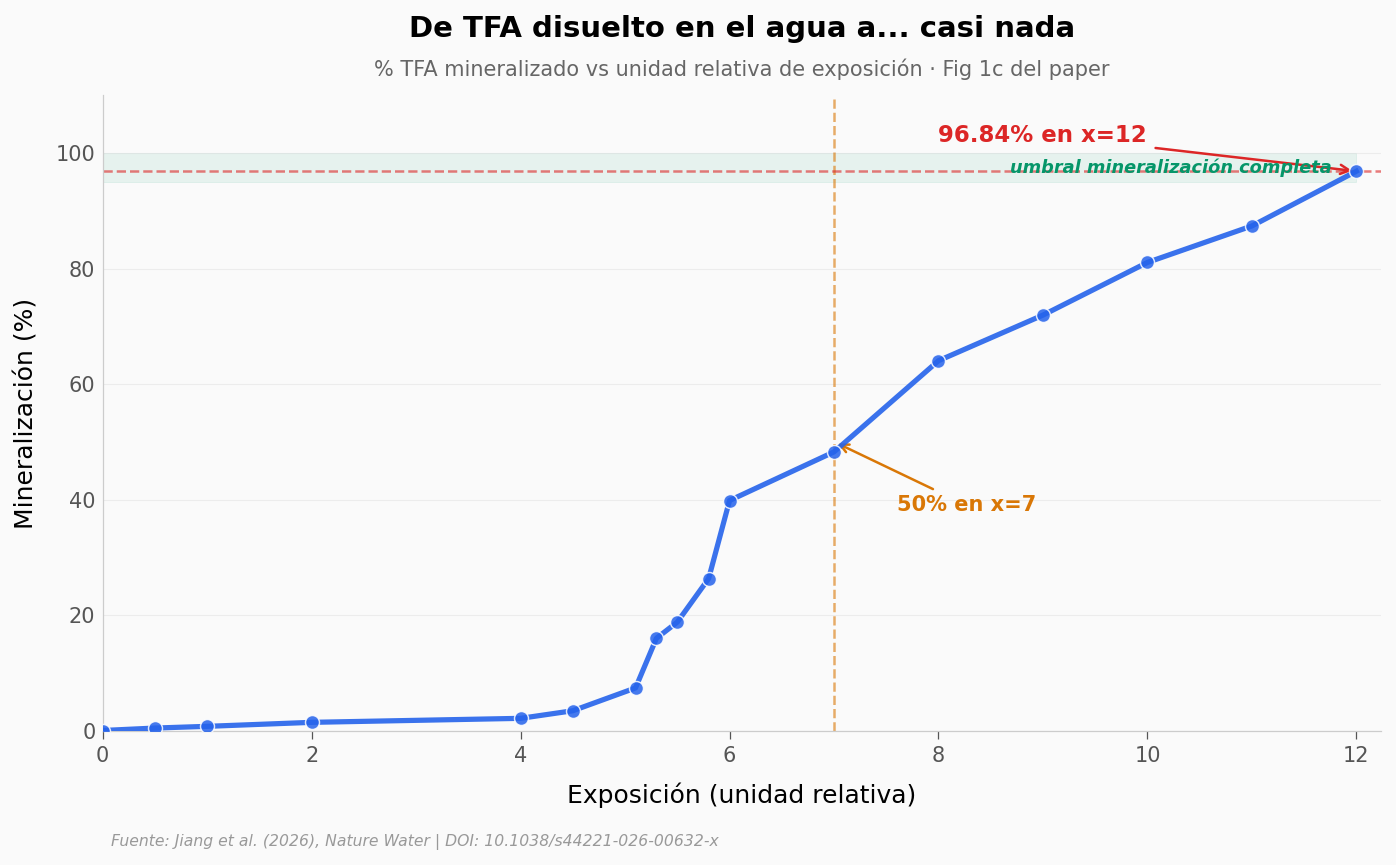
Mineralización máxima alcanzada: 96.84% (en x=12)
Punto de 50% mineralización: x=7
Para ponerlo en perspectiva: las estrategias previas con •OH solo conseguían
defluorinaciones parciales (≪50%) en TFA bajo condiciones similares.
Lo que los datos soportan#
Afirmación |
¿Soportada? |
Detalle |
|---|---|---|
El radical O•⁻ ataca al TFA con k ≈ 5.1 × 10⁷ M⁻¹ s⁻¹ |
✅ |
Nuestro ajuste lineal sobre 4 concentraciones (2–20 mM) da 5.14 × 10⁷ M⁻¹ s⁻¹ — coincide dentro del 1% con lo reportado |
El método logra mineralización casi completa del TFA |
✅ |
La curva de la Fig 1c llega a 96.84% en el punto máximo medido (x=12) — esencialmente mineralización completa dentro del rango medido |
Funciona también con PFBA, PFHxA y PFOA |
⚠️ |
El paper lo demuestra en su Fig 3 con 4 substratos perfluorados; este Lab solo abre los datos del TFA |
El O•⁻ es 50 veces más rápido que el electrón hidratado |
⚠️ |
Cita literal del abstract — la cinética del e_aq⁻ se mide en una serie distinta de experimentos no incluida en este notebook |
Aplicable a tasas industriales de hasta 0.27 mol L⁻¹ h⁻¹ |
⚠️ |
Reportado en el paper con electron beam comercial; depende de la dosis efectiva entregada al volumen de agua, que varía por reactor |
Limitaciones:
Solo 4 puntos en la curva cinética → la incertidumbre del slope no es despreciable, pero el ajuste es coherente con el valor del paper.
El eje x de la curva de mineralización es una «unidad relativa» — el paper no especifica unívocamente si es dosis (kGy) o tiempo. La interpretación cualitativa (0→97%) es robusta; la velocidad absoluta no.
La curva de mineralización mide TFA puro en agua deionizada. La gráfica de iones muestra que la presencia de NO₃⁻ o CO₃²⁻ degrada fuertemente el rendimiento: en agua real, el techo del 97% probablemente baja.
No hay réplicas reportadas en los datos abiertos para construir intervalos de confianza por punto.
Ahora tú#
Tres preguntas para abrir los datos por tu cuenta:
¿Qué pasa si recortas el rango de [TFA] a 2–10 mM? El cuarto punto (20 mM) es el más alto y puede estar dominando el slope. Sin él, ¿k(O•⁻+TFA) sigue dando ≈5×10⁷?
cinetica_o.iloc[:3]El nitrato apaga la reacción al 0.8%. ¿Cuánto nitrato hay en agua de la llave típica? Búscalo en datos públicos (la EPA fija el límite en 10 mg/L). Compáralo con la concentración usada en el experimento (10 mM ≈ 620 mg/L → ~62× el límite EPA).
¿Qué tasa de mineralización se necesitaría para limpiar 1 m³ de agua contaminada con 100 ng/L de TFA? Pista: convierte ng/L a M, multiplica por 1000 L, divide por la tasa industrial (0.27 mol L⁻¹ h⁻¹). El resultado es sorprendente.
# --- EXPERIMENTA AQUÍ ---
# Pregunta: ¿cuánto tiempo tomaría limpiar 1 m³ de agua contaminada con 100 ng/L de TFA
# usando la tasa industrial reportada (0.27 mol/L/h)?
import math
masa_molar_tfa = 114.02 # g/mol (CF₃COOH)
volumen_litros = 1000 # 1 m³ = 1000 L
concentracion_inicial_ng_l = 100
tasa_mol_l_h = 0.27 # tasa industrial reportada (electron beam comercial)
# Concentración inicial en mol/L
ng_to_g = 1e-9
c_mol_l = (concentracion_inicial_ng_l * ng_to_g) / masa_molar_tfa
print(f"Concentración inicial: {c_mol_l:.2e} M")
# Moles totales en el volumen
moles_totales = c_mol_l * volumen_litros
print(f"Moles totales de TFA: {moles_totales:.2e} mol")
# Tiempo a tasa industrial
tiempo_horas = c_mol_l / tasa_mol_l_h
tiempo_segundos = tiempo_horas * 3600
print(f"\nTiempo para mineralizar a {tasa_mol_l_h} mol/L/h: {tiempo_segundos*1000:.3f} ms")
print("\nEs decir: la tasa industrial está varios órdenes de magnitud por encima de lo")
print("que se necesita para concentraciones reales de TFA en aguas naturales.")
print("La pregunta práctica deja de ser '¿alcanza?' y se convierte en '¿a qué costo")
print("energético del e-beam y a qué escala?'.")
Concentración inicial: 8.77e-10 M
Moles totales de TFA: 8.77e-07 mol
Tiempo para mineralizar a 0.27 mol/L/h: 0.012 ms
Es decir: la tasa industrial está varios órdenes de magnitud por encima de lo
que se necesita para concentraciones reales de TFA en aguas naturales.
La pregunta práctica deja de ser '¿alcanza?' y se convierte en '¿a qué costo
energético del e-beam y a qué escala?'.
Créditos#
Notebook generado como parte del Lab de Ciencia a Mordiscos.
Repo: github.com/Ciencia-a-Mordiscos/lab · Licencia: CC BY 4.0
Fuentes#
Paper: The O•−/electron tandem path for complete mineralization of trifluoroacetate and perfluorocarboxylic acids
Nature Water, 2026-04-15
Supplementary Information: Nature Water (Supplementary)
Datos: Figshare
15 afirmaciones verificadas contra estas fuentes